Basalganglien
Die Basalganglien bestehen aus 4 Hauptformationen, bestehend aus:
- gestreifter
- globus pallidus
- substantia nigra (bestehend aus einer Pars compacta und einer Pars reticulata)
- Nucleus subthalamicus
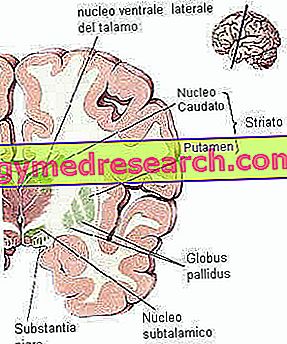
Koronale Schnittdarstellung der Basalganglien (Quelle h ttp: //mindblog.dericbownds.net/)
Das Striatum wiederum besteht aus dem kaudalen Kern, Putamen und dem ventralen Striatum, zu denen der Nucleus accumbens gehört.
Das Striatum ist wichtig, weil es die Hauptafferenzen der Kerne der Basis, der Großhirnrinde, des Thalamus und des Rumpfes des Enzephalons, aufnimmt (Abbildung 1). Seine Neuronen projizieren zum Globus Pallidus und zur Substantia Nigra.
Von diesen beiden Kernen, deren Neuronen morphologisch ähnliche Somes oder Körper haben, stammen die Hauptprojektionen der Kerne der Basis.
Streak-Funktionen
Das Striatum besteht aus zwei verschiedenen Teilen, den Kompartimenten Matrix und Striosomen. Diese Kompartimente haben unterschiedliche histologische Merkmale und unterschiedliche Rezeptoren. Das Striosomenkompartiment empfängt Afferenzen hauptsächlich aus dem limbischen Kortex und ragt hauptsächlich in die Pars compacta der Substantia nigra hinein. Um die Funktionsweise des Striatums besser zu verstehen, sollte erwähnt werden, wie die Schaltung oder die Kommunikation zwischen den verschiedenen Gehirnbereichen funktioniert.
Alle Bereiche der Großhirnrinde senden exzitatorische glutamaterge Projektionen an bestimmte Bereiche des Striatum. Das Striatum empfängt auch exzitatorische Signale von den intralaminaren Kernen des Thalamus, dopaminerge Projektionen vom Mittelhirn und serotoninerge von den Raphekernen.
Insbesondere besteht das Striatum aus verschiedenen Zelltypen, aber 90-95% der Zellen, aus denen es besteht, bestehen aus GABAergen Projektionsneuronen. Sie stellen das Hauptziel von Projektionen dar, die von der Großhirnrinde ausgehen, und sind auch die einzige Quelle efferenter Projektionen. Normalerweise sind sie stille Neuronen, außer während der Bewegung oder nach der Anwendung peripherer Reize. Das Striatum besteht auch aus lokalen inhibitorischen Interneuronen, die dank ihrer entwickelten axonalen Kollateralen die Aktivität der efferenten striatalen Neuronen verringern. Obwohl diese Neuronen in geringen Mengen vorhanden sind, sind sie für den größten Teil der tonischen Aktivität des Striatum verantwortlich.
Was die Schaltkreise betrifft, so ragt das Striatum über zwei Wege zu den Kernen, von denen die efferenten Pfade ausgehen: über einen direkten Pfad, der anregend ist, und einen indirekten Pfad eines inhibitorischen Typs.
So tragen die Basalganglien durch Wechselwirkungen mit der Großhirnrinde zur freiwilligen Bewegung, aber auch zu anderen Verhaltensweisen wie Skelettmotorik, Okulomotorik, kognitiven und emotionalen Funktionen bei. Beispielsweise wurde bei einigen Personen mit Huntington-Krankheit beobachtet, dass einige Läsionen auf der Ebene der Kerne der Basis negative emotionale und kognitive Effekte hervorrufen.
Neuropathologie der Huntington-Krankheit
Pathologisch äußert sich die Huntington-Krankheit in einer Atrophie des Striatum, das, wie im vorherigen Abschnitt beschrieben, aus Caudate und Putamen besteht. Eine Atrophie verursacht einen neuronalen Verlust, der auch mit einem Zustand der Gliose (einem Prozess der Astrozytenproliferation in beschädigten Bereichen des Gehirns) verbunden ist. 1985 stufte der Gelehrte Vonsattel diese Krankheit in Bezug auf das Ausmaß der Striatalatrophie von Grad 0 (wo keine Veränderungen auftreten) in Grad 4 ein. Es wurde auch gezeigt, dass der Grad der Atrophie, der auf der Ebene des Striatum auftritt, auch mit der Degeneration anderer nicht-striataler Hirnstrukturen korreliert.
Im Striatum sind die am stärksten betroffenen Neuronen die Neuronen des stacheligen Mediums, die die größte Population im Striatum darstellen und die GABA, eine Aminosäure vom inhibitorischen Typ, als Neurotransmitter verwenden.
Es wurde auch gezeigt, dass die Huntington-Krankheit durch das Vorhandensein intraneuronaler Einschlüsse und Proteinaggregate in dystrophen Axonen sowie in striatalen und kortikalen Neuronen gekennzeichnet ist; Es ist ein Phänomen, das auch bei anderen Polyglutamin-Erkrankungen (dh Triplett-Expansionen, wie im Fall der Huntington-Krankheit) auftritt. Es wurde auch beobachtet, dass sich intranukleäre Einschlüsse vor dem Abnehmen des Gehirns, aber auch vor dem Abnehmen des Körpergewichts und vor dem Auftreten neurologischer Symptome manifestieren.



