Allgemeinheit
Mitralinsuffizienz (oder Mitralinsuffizienz ) besteht aus dem unvollständigen Schließen der linken atrioventrikulären Öffnung, in der sich die Mitralklappe (oder Mitralklappe) befindet; dies geschieht während der Phase der ventrikulären Systole, dh im Moment der Kontraktion der Herzventrikel; Unter ähnlichen Bedingungen kehrt das Blut vom linken Ventrikel zum linken Vorhof zurück, wenn die Öffnung aufgrund von Klappeninkontinenz nicht vollständig geschlossen ist. Dies ist die sogenannte Mitralinsuffizienz.
Die Ursachen für eine Mitralklappeninsuffizienz sind zahlreich und können eine oder mehrere Komponenten der Mitralklappe verletzen. Die Symptome sind, obwohl weniger offensichtlich, denen der Mitralstenose sehr ähnlich: Dyspnoe, Vorhofflimmern und Schwäche, um nur einige zu nennen.
Zur Diagnose der Mitralinsuffizienz werden verschiedene instrumentelle Methoden eingesetzt: Elektrokardiographie, Echokardiographie, Röntgenuntersuchung der Brust und Herzkatheteruntersuchung haben jeweils unterschiedliche Vorteile bei der Beurteilung des Ausmaßes der Herzerkrankung. Die Behandlung hängt von der Schwere des Mitralversagens ab: Wenn die Situation kritisch ist, ist eine Operation erforderlich.
Was ist Mitralinsuffizienz?
Pathologische Anatomie und Pathophysiologie
Mitralinsuffizienz, auch Mitralinsuffizienz genannt, besteht aus dem unvollständigen Verschluss der linken atrioventrikulären Öffnung, der die Mitralklappe (oder Mitralklappe) vorsteht.
Unter normalen Bedingungen verschließt die Mitralklappe während der Ventrikelsystole (wenn sich der Ventrikel zusammenzieht) den Durchgang zwischen Vorhof und Ventrikel hermetisch. infolgedessen fließt das Blut nur in eine Richtung zur Aorta.
Bei Mitralinsuffizienz tritt das pathologische Ereignis genau in der Phase der Ventrikelsystole auf: Wenn sich der Ventrikel zusammenzieht, dreht sich ein Teil des Blutes zurück und geht zurück in den oberen linken Vorhof. Aus diesem Grund wird Mitralinsuffizienz auch als Mitralinsuffizienz bezeichnet.
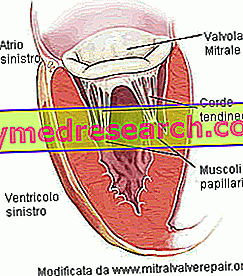
Bevor untersucht wird, wie eine Mitralklappe bei Mitralinsuffizienz aussieht und funktioniert (Analyse der pathologischen Anatomie bzw. Physiopathologie), sollten einige grundlegende Merkmale der Klappe erwähnt werden:
- Der Ventilring . Umfangsstruktur des Bindegewebes, das die Klappenöffnung definiert.
- Die Ventilöffnung hat einen Durchmesser von 30 mm und eine Oberfläche von 4 cm2.
- Zwei Klappen vorne und hinten. Aus diesem Grund wird gesagt, dass die Mitralklappe bikuspid ist . Beide Klappen passen in den Klappenring und blicken in Richtung Kammerhöhle. Die vordere Packungsbeilage zeigt zur Aortenöffnung; der hintere Lappen zeigt stattdessen auf die Wand des linken Ventrikels. Die Lappen bestehen aus Bindegewebe, das reich an elastischen Fasern und Kollagen ist. Um das Verschließen der Öffnung zu erleichtern, weisen die Ränder der Klappen besondere anatomische Strukturen auf, die als Kommissuren bezeichnet werden. Es gibt keine direkten Kontrollen nervöser oder muskulöser Art an den Klappen. Ebenso gibt es keine Vaskularisation.
- Die papillären Muskeln . Sie sind zwei und sind Erweiterungen der ventrikulären Muskulatur. Sie werden von den Herzkranzgefäßen gesprüht und geben den Sehnensträngen Stabilität.
Bei Vorliegen einer Mitralinsuffizienz aufgrund der auslösenden Ursache kommt es zu Verletzungen an einer oder mehreren dieser Klappenkomponenten. Basierend auf den durch jede Ursache ausgelösten Effekten wurden zwei Arten von Mitralinsuffizienz unterschieden, die jeweils unterschiedliche physiopathologische Verhaltensweisen gruppierten. Deshalb haben wir:
- Akute Mitralklappeninsuffizienz.
- Chronische Mitralinsuffizienz.
Der Unterschied zwischen der akuten und der chronischen Form hängt zuallererst von der Schnelligkeit ab, mit der die Kardiopathie selbst festgestellt wird. Bevor wir jedoch auf diesen Punkt eingehen, müssen wir einige physiopathologische Aspekte klären, die beiden Formen gemeinsam sind.
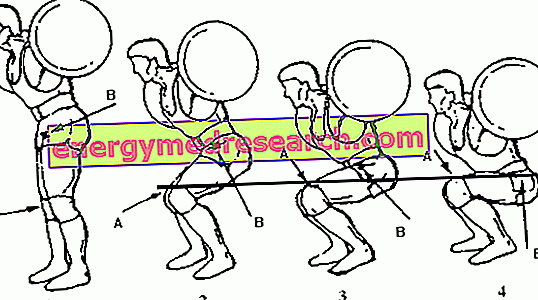
Bei Mitralinsuffizienz beeinflussen sowohl der linke Vorhof als auch der linke Ventrikel die pathologische Anpassung des Blutflusses. Unter normalen Bedingungen stellt der hermetische Verschluss der Mitralklappe während der Ventrikelsystole die Gleichrichtung des Blutflusses zur Aorta sicher. Bei Mitralinsuffizienz pumpt der linke Ventrikel das Blut jedoch in zwei Richtungen: Aorta (richtige Richtung) und linker Vorhof (falsche Richtung aufgrund von Klappeninkontinenz). Daher verringert sich der Anteil des Bluts, der das Gewebe erreicht, und seine Durchflussrate variiert je nach Größe der Öffnung: Je weniger effizient der Mitralverschluss ist, desto mehr Blut fließt in den Vorhof zurück (aufgestaute Fraktion). und das Herzzeitvolumen ist niedriger. Darüber hinaus erweitert sich der linke Vorhof entsprechend, um die größten Blutmengen aufzunehmen.
Während der Diastole, das heißt in der Entspannungsphase von Ventrikeln und Vorhöfen, kehrt das aufgestaute Blut (im Vorhof) zum Ventrikel zurück, da sich die Mitralklappe in dieser Phase öffnet.
Diese letzte abnormale Blutbewegung und das vorherige Aufstoßen haben Auswirkungen auf den atrioventrikulären Druckgradienten . Gradient bedeutet in diesem Fall eine Veränderung des Drucks. Tatsächlich weicht das zwischen den beiden Kompartimenten bestehende Druckverhältnis bei Vorliegen einer Mitralstenose vom Normalwert ab. Die Druckänderungen sind auf den Anteil des aufgestauten Blutes zurückzuführen, der zunächst im Vorhof und dann im Ventrikel zu dem aus dem normalen Blutkreislauf stammenden Anteil hinzugerechnet wird. Dies geschieht zu falschen Zeiten und führt zu einem Anstieg des ventrikulären Drucks. In diesem Fall spricht man von linksventrikulärem Versagen .
Wenn die Ursache der Mitralinsuffizienz dieses eben beschriebene Szenario langsam bestimmt, kann sich der linke Ventrikel an die Veränderungen anpassen ( chronische Form ): Er wird hypertroph, so dass der Druckanstieg in ihm unter Kontrolle bleibt. Tatsächlich gleichen die hypertrophen ventrikulären Wände zum Zeitpunkt der Kontraktion die beträchtliche Spannung aus, die durch den hohen Druck und die wiederaufgestaute Höhe verursacht wird, und bleiben stabil. Diese Situation führt jedoch zu einer langsamen Verschlechterung der Ventrikelwände, die zu einer Abnahme des Herzzeitvolumens führen soll.
Wenn die Ursache der Mitralinsuffizienz andererseits die oben beschriebenen physiopathologischen Mechanismen rasch entwickelt, hat der linke Ventrikel nicht genügend Zeit, sich an die Veränderung anzupassen, und wird nicht hypertrophisch ( akute Form ). Die Wände des Ventrikels sind daher aufgrund des hohen Drucks nicht in der Lage, der Spannung zu widerstehen, und das Ausmaß der Blutinsuffizienz nimmt zunehmend zu. Dies führt zu einem kontinuierlichen Druckanstieg im linken Vorhof, der sich auf die vorgelagerten Gefäße und Bezirke, die Lungenvenen und die Lunge auswirkt und möglicherweise zu Ödemen führt.
Ursachen
Die Ursachen für Mitralinsuffizienz sind zahlreich. Jedes von ihnen verursacht Läsionen eines oder mehrerer struktureller Elemente, aus denen die Mitralklappe besteht. manchmal kann es vorkommen, dass zwei verschiedene Ursachen, die sich addieren, eine Läsion von nur einer Ventilkomponente ergeben.
Bei akuter Mitralinsuffizienz:
| Art der Verletzung | Ursache |
Veränderungen des Mitralrings Veränderungen der Klappenblätter Bruch der Sehnenbänder Papilläre Muskelstörungen | Infektiöse Endokarditis; Trauma; akute rheumatische Erkrankung; idiopathische; Myxomatose-Degeneration (Kollagenopathie); koronare Herzkrankheit; Fehlfunktion der Klappenprothese. |
Bei chronischer Mitralinsuffizienz:
| Art der Verletzung | Ursache |
Veränderungen des Mitralrings Veränderungen der Klappenblätter Bruch der Sehnenbänder Papilläre Muskelstörungen | entzündliche; rheumatische Herzkrankheit; Verkalkung; Myxomatose-Degeneration (Kollagenopathie); infektiöse Endokarditis; Herzischämie; Marfan-Syndrom (angeboren); Klappenriss (angeboren); Mitralklappenprolaps (angeboren); Bindegewebe. |
Die beiden Formen der Mitralinsuffizienz haben daher nur einige gemeinsame Ursachen.
Symptome und Anzeichen
Die Hauptsymptomatik der Mitralinsuffizienz ist zwar weniger offensichtlich, weist jedoch viele Ähnlichkeiten mit derjenigen auf, die die Mitralstenose charakterisiert.
- Dyspnoe bei Anstrengung.
- Kardiopalmus (Herzklopfen).
- Infektionen der Atemwege.
- Asthenie.
- Schmerzen in der Brust aufgrund von Angina Pectoris.
- Lungenödem.
Mühelose Atemnot besteht aus Atembeschwerden. Im konkreten Fall ergibt sich dies aus der Abnahme des Herzzeitvolumens des linken Ventrikels aufgrund des zum Atrium zurückgeworfenen Blutanteils. Daher besteht die Reaktion des Organismus darin, die Anzahl der Atemzüge zu erhöhen, um die verringerte Sauerstoffzufuhr aufgrund des unzureichenden Bereichsvolumens auszugleichen.
Ein Lungenödem ist ein typisches Symptom für eine akute Mitralklappeninsuffizienz. Das rasche Einsetzen von Herzerkrankungen erlaubt es dem Ventrikel nicht, die durch erhöhten ventrikulären Druck induzierten Wirkungen zu begrenzen. Anders als bei chronischer Insuffizienz hat der linke Ventrikel tatsächlich keine Zeit, hypertrop zu werden. Infolgedessen steigt der Anteil des aufgestauten Blutes progressiv an. Dies führt zu einem Druckanstieg nicht nur im linken Vorhof, sondern auch in den vorgelagerten Gefäßen und Bezirken, dh Lungenvenen und Lungen . Der erhöhte Lungendruck (pulmonale Hypertonie ) führt zu einer Kompression der Atemwege und im schlimmsten Fall zum Austreten von Flüssigkeiten aus den Gefäßen in die Alveolen. Dieser letzte Zustand ist der Auftakt zum Lungenödem: Unter diesen Bedingungen ist der Sauerstoff-Kohlendioxid-Austausch zwischen Alveolen und Blut beeinträchtigt.
Herzkrankheiten, auch Herzklopfen genannt, sind das häufigste Symptom für Mitralinsuffizienz. Es besteht aus einer Erhöhung der Intensität und Frequenz des Herzschlags. Im konkreten Fall kann eine Herzinsuffizienz auf Vorhofflimmern zurückzuführen sein
Vorhofflimmern ist eine Herzrhythmusstörung, dh eine Veränderung des normalen Herzrhythmus. Es ist auf eine Störung des Nervenimpulses zurückzuführen, der vom Sinusknoten des Vorhofs ausgeht. Es kommt zu fragmentarischen und ineffektiven atrialen Kontraktionen aus hämodynamischer Sicht (dh was die Durchblutung betrifft).
Bei Mitralinsuffizienz verändert das Aufstoßen von Blut im Atrium das Blutvolumen, das durch ventrikuläre Kontraktion in die Aorta gedrückt wird. Vor diesem Hintergrund wird der Sauerstoffbedarf des Körpers nicht mehr gedeckt. Angesichts dieser Situation verstärkt das an Vorhofflimmern leidende Individuum die Atmungsaktivität, manifestiert Herzklopfen, Unregelmäßigkeiten des Handgelenks und fällt in einigen Fällen aufgrund von Luftmangel in Ohnmacht. Das Bild kann weiter degenerieren: Eine stetig zunehmende Regurgitation und die Ansammlung von Blut in den vaskulären Systemen vor dem linken Vorhof führen, wenn sie mit einer veränderten Koagulation einhergehen, zur Bildung von Thromben (feste, nicht bewegliche Massen, bestehend aus Blutplättchen) in den Gefäßen. Die Thromben können sich auflösen und Partikel, sogenannte Emboli, freisetzen, die im Gefäßsystem das Gehirn oder das Herz erreichen können. An diesen Stellen behindern sie das normale Versprühen und die Sauerstoffversorgung des Gehirns oder des Herzgewebes und verursachen den sogenannten ischämischen Schlaganfall (zerebral oder kardial). Beim Herzen spricht man auch von einem Herzinfarkt .
Im Gegensatz zu Mitralstenosen sind Embolien aufgrund von Mitralinsuffizienz seltener.
Infektionen der Atemwege oder des Brustraums sind auf ein Lungenödem zurückzuführen.
Brustschmerzen aufgrund von Angina Pectoris sind selten. Angina pectoris ist auf eine linksventrikuläre Hypertrophie zurückzuführen, dh auf den linken Ventrikel. Tatsächlich benötigt das hypertrophe Myokard mehr Sauerstoff, aber dieser Wunsch wird vom Koronarimplantat nicht ausreichend unterstützt. Es ist daher nicht die Folge einer Verstopfung der Herzkranzgefäße, sondern eines Ungleichgewichts zwischen dem Verbrauch und der Versorgung des Gewebes mit Sauerstoff.
Das charakteristische klinische Zeichen einer Mitralinsuffizienz ist das systolische Rauschen . Es entsteht durch das Aufstoßen von Blut durch die halboffene Klappe während der ventrikulären systolischen Kontraktion.
Diagnose
Mitralinsuffizienz kann durch die folgenden diagnostischen Tests festgestellt werden:
- Stethoskopie.
- Elektrokardiogramm (EKG).
- Echokardiographie.
- Thorax Radiographie.
- Herzkatheterisierung.
Stetoskopie . Die Erkennung eines systolischen Geräusches ist die nützlichste Indikation zur Diagnose einer Mitralklappeninsuffizienz. Das Geräusch des Atems wird durch den Übergang von der linken Herzkammer zum linken Vorhof durch das Aufstoßen von Blut erzeugt. Es wird in der systolischen Phase wahrgenommen, da zu diesem Zeitpunkt die Mitralklappe nicht wie gewünscht geschlossen ist. Ein starker Atemzug weist auf eine mäßige, aber nicht unbedingt starke Insuffizienz hin. Tatsächlich wird ein schwacher Atem sowohl bei Personen mit leichter Mitralinsuffizienz als auch bei Personen mit schwerer (dh schwerer) Insuffizienz wahrgenommen. Diese letzte Situation ist die Folge einer fortschreitenden Degeneration des linken Ventrikels. Die Erkennungszone befindet sich im V-Interkostalraum, dh der Zone, die mit der Position der Mitralklappe übereinstimmt.
EKG . Durch Messung der elektrischen Aktivität eines Herzens mit Mitralinsuffizienz zeigt das EKG:
- Hypertrophie des linken Ventrikels.
- Überlastung des linken Atriums.
- Vorhofflimmern.
- Herzischämie.
Die EKG-Diagnose gibt Aufschluss über den Schweregrad des Mitralversagens: Wenn das Ergebnis mit dem eines gesunden Menschen vergleichbar ist, bedeutet dies, dass es sich nicht um eine schwere Form handelt. Umgekehrt zeigt die Untersuchung die genannten Unregelmäßigkeiten.
Echokardiographie . Dieses Diagnosetool nutzt die Ultraschallemission und zeigt auf nicht-invasive Weise die grundlegenden Elemente des Herzens: Vorhöfe, Ventrikel, Klappen und umgebende Strukturen. Mit Hilfe der Echokardiographie kann der Arzt Folgendes feststellen:
- Anormales Verhalten der Klappen aufgrund einer Beschädigung der Sehnenstränge der Klappe.
- Anomalien des linken Ventrikels während der Phasen Systole und Diastole.
- Vergrößerung des linken Vorhofs (erweiterter Vorhof).
- Die maximale Strömungsgeschwindigkeit ist die turbulente systolische Strömung der Regurgitation unter Verwendung kontinuierlicher bzw. gepulster Doppler-Techniken. Aus der ersten Messung kann der Druckgradient zwischen dem linken Vorhof und dem linken Ventrikel abgeleitet werden; ab dem zweiten das Ausmaß des Aufstoßen.
Röntgenaufnahme der Brust . Es ist nützlich, um die Situation auf Lungenebene zu beobachten und um festzustellen, ob Ödeme vorliegen oder nicht. Darüber hinaus können typische anatomisch-pathologische Veränderungen beobachtet werden:
- Linksatrium durch Aufstoßen von Blut erweitert.
- Hypertrophe linke Herzkammer.
- Verkalkung, bestimmt durch bestimmte Ursachen des Ventils oder Rings.
Herzkatheterisierung . Es ist eine invasive hämodynamische Technik. Ein Katheter wird in das Gefäßsystem eingeführt und zum Herzen geführt. In den Gefäß- und Herzhöhlen fungiert es als Untersuchungssonde. Die Zwecke dieser Prüfung sind wie folgt:
- Bestätigen Sie die klinische Diagnose.
- Bewerten Sie die hämodynamischen Veränderungen, dh den Blutfluss in Gefäßen und Herzhöhlen, quantitativ. Insbesondere wird der Zustand auf Lungenebene untersucht.
- Definieren Sie sicher, ob Sie chirurgisch eingreifen können.
- Bewerten Sie das mögliche Vorhandensein anderer Ventilstörungen.
Therapie
Der therapeutische Ansatz variiert je nach Schweregrad der Mitralinsuffizienz. Die milden, asymptomatischen Formen erfordern vorbeugende Maßnahmen, um bakterielle Infektionen wie Endokarditis, die die Herzhöhlen betreffen, zu verhindern.
Das erste Auftreten von Symptomen und mittelschweren / schweren Formen erfordert mehr Aufmerksamkeit durch medikamentöse Therapie und möglicherweise Operation.
Die am häufigsten verwendeten Medikamente bei symptomatischen Fällen von Mitralinsuffizienz sind:
- ACE-Hemmer . Sie sind Inhibitoren des Enzymsystems, das Angiotensin umwandelt. Es handelt sich um blutdrucksenkende Medikamente, die den erhöhten Druck in den linksatrioventrikulären Hohlräumen und den stromaufwärts gelegenen Gefäßsystemen verringern.
- Diuretika . Sie sind auch blutdrucksenkend.
- Vasodilatatoren . Beispiel: Nitroprussid.
- Digital . Es wird für Vorhofflimmern verwendet.
In einigen kritischen Situationen ist eine Operation unerlässlich: wenn der Patient an einer schweren Form einer chronischen Mitralinsuffizienz leidet oder an einer akuten Form leidet.
Es gibt zwei mögliche chirurgische Eingriffe:
- Ersatz der Klappe durch eine Prothese . Es ist die am häufigsten durchgeführte Intervention für die Klappen dieser nicht jungen Personen mit schwerwiegenden anatomischen Anomalien. Eine Thorakotomie wird durchgeführt und der Patient in einen extrakorporalen Kreislauf (CEC) gebracht. Die extrakorporale Zirkulation wird durch ein biomedizinisches Gerät erreicht, das darin besteht, einen kardiopulmonalen Weg zu schaffen, der den natürlichen ersetzt. Auf diese Weise wird dem Patienten eine künstliche und vorübergehende Durchblutung garantiert, die es dem Chirurgen ermöglicht, den Blutfluss im Herzen zu unterbrechen und ihn auf einen anderen, gleichermaßen wirksamen Weg umzuleiten. Gleichzeitig können Sie die Ventilvorrichtung frei bedienen. Prothesen können mechanisch oder biologisch sein. Mechanische Prothesen erfordern parallel eine gerinnungshemmende Arzneimitteltherapie. Biologische Prothesen halten 10-15 Jahre.
- Reparatur der Mitralklappe . Es ist ein Ansatz, der bei Mitralinsuffizienz aufgrund von Veränderungen der Klappenstrukturen angezeigt ist: Ring, Eckzähne, Sehnenbänder und Papillarmuskeln. Der Chirurg verhält sich je nachdem, wo sich die Klappenläsion befindet, unterschiedlich. Auch hier werden die Patienten in den extrakorporalen Kreislauf gebracht. Es ist eine vorteilhafte Technik, da die Prothesen einige Nachteile aufweisen: Wie wir gesehen haben, müssen die biologischen nach etwa 10 bis 15 Jahren ersetzt werden, während die mechanischen die kontinuierliche parallele Verabreichung von Antikoagulanzien erfordern. Es ist eine Methode, die für die rheumatischen Formen der Mitralinsuffizienz nicht geeignet ist: Diese sind jedoch selten.